Sempre é difícil começar um post novo, nunca sei exatamente o que falar no início. Mas vamos ao breve surgimento da ideia, como sempre faço, né? 🙂 Antes de começar a graduação havia encontrado sugestões na internet para séries e documentários relacionados à Química e um deles era o Química: Uma História Volátil.

Nossa, quando assisti me apaixonei! Abaixo trouxe o trailer. Infelizmente aparece esse anúncio chato de 30 segundos no começo!
–
Esse documentário é incrível, ainda mais pra mim naquela época, recém-egressa do Ensino Médio e com pouquíssimo contato com os processos realizados para as descobertas relacionadas ao mundo químico! Assistir essa belíssima produção foi motivador para que eu me interessasse também pela História da Química ❤, porque até então, pelo que me lembro, não ligava muito para essa área.

–
Acho que não me interessava por esse ramo porque nas aulas também não trabalhávamos o contexto histórico da Química, né? Só víamos o pequeno box no livro didático dizendo que determinado cientista genial tinha descoberto algo relevante e pronto.
Enfim, quando cursei no início da graduação a disciplina de História da Ciência, novamente tive contato com este documentário ao ser transmitido para a turma. O pessoal também gostou! 😉 Para assistir ao primeiro episódio de três, você pode clicar aqui ou assistir abaixo mesmo. Mas caaalma! Continue lendo o post primeiro! 😀
https://dailymotion.com/video/x2e4n65
–
Só que eu tive um probleminha. Após ter assistido essas duas vezes aos três vídeos que compõem a série, percebi que ainda tenho dificuldades para lembrar exatamente quais são as informações transmitidas pelo filme e em qual episódio elas estão. Isso porque os três vídeos trazem histórias, fatos e experimentos de vários cientistas e lugares, de épocas diversas. Me diga, então, se não é uma pena, isso de esquecer essas informações que poderiam ser aproveitadas nas aulas de Química, seja passando o documentário inteiro ou trechos específicos!

–
Por esse motivo, pensei em reescrever algumas partes importantes da narração contida em “A descoberta dos elementos”, que é o primeiro episódio da série em questão. Só posso dizer que foi desafiador, haha, vários dias escrevendo. Acho que foi ainda mais trabalhoso pra quem traduziu e legendou o vídeo. Parabéns! Uma vez legendei esse vídeo de Breaking Bad de 5 minutos e quase morri. XD
Enfim, mas pensei em transcrever porque acho que ajudaria muito a mim e a você, caso estivesse procurando um trecho já assistido. Seria um desperdício deixarmos de utilizar esse material por não lembrarmos exatamente de tudo que esses episódios tratam!
Assim, caso você não disponha no momento de 58 minutos para conferir o primeiro episódio inteiro, você também pode dar uma olhadinha nessa parte escrita abaixo que está mais adiante nesse post com imagens OOOU no PDF pra download sem as imagens. Só não deixe de assistir ao vídeo, né? 😀 Pode ser útil passar trechos ou o vídeo inteiro em sua aula. Abaixo também se encontra um link para download do vídeo compartilhado pelo professor João Paulo Santos.
Downloads
– Química: Uma História Volátil – 3 episódios (Baixar vídeos)
– A descoberta dos elementos – 1º episódio (Post atual · Baixar texto PDF)
– A ordem dos elementos – 2º episódio (Ver post · Baixar texto PDF)
– O poder dos elementos – 3º episódio – Em breve!
Não encontrei em nenhuma loja para vender os DVDs, só nessa loja DVDs Científicos, por R$30. Nunca comprei nela, então não tenho uma opinião formada. Mas achei válido compartilhar com vocês o link. Caso queiram comprar os DVDs, clique aqui.

–
Me conte nos comentários aqui abaixo se você já assistiu e o que achou, SE usaria e COMO usaria em sua aula! Vamos, todos os profs, nos ajudar nesse mundo internético! 🙂 Se você é aluno, pode deixar sua sugestão também. Por favor, comentem… Porque às vezes me sinto falando sozinha nesse blog.

–
Como o post é beeeeeeem longo por causa dos trechos com imagens, você pode clicar aqui para deixar seu comentário.
A seguir trouxe para vocês alguns dos assuntos abordados no vídeo, como disse anteriormente, juntamente com os minutos em que aparecem. Fiz isso para facilitar a identificação dos trechos quando você for procurar e planejar sua aula, e não com o objetivo de fazer parecer que os escritos abaixo são de minha total autoria, como se tivesse pensado em tudo sozinha. Se for procurar uma palavra em específico digite Ctrl + F escreva a palavra! Esse atalho é VIDA. ❤
–
Química: Uma História Volátil – A descoberta dos elementos (Episódio 1 de 3)
(00:00) A descoberta dos elementos começa com o apresentador Jim Al-Khalili buscando entender do que tudo no nosso mundo é feito e qual foi a construção do conhecimento acerca disso, principalmente a relativa ao mundo químico. Menciona que os antigos gregos já conheciam o chumbo, cobre, ouro, prata, ferro, mercúrio e estanho, mas que os consideravam apenas metais, feitos de terra, ar, fogo e água, os quatro elementos. Só a partir dos últimos 200 anos que foi sendo descoberto o que são os elementos, porque por mais de mil anos não tivemos meios para desvendar a natureza e não tínhamos outra escolha senão basear nosso conceito de elementos no que era visível ao nosso redor.

–
(04:09) Isso começou ali depois do século 16, com os alquimistas e suas anotações secretas, tentando transformar metais em ouro e sonhar com a imortalidade. Segundo o vídeo, foi um alquimista que primeiramente desafiou a ideia de que tudo era feito desses quatro elementos. Sua história começa em Basileia, na Suíça, com Philippus Aureolus Theophrastus Bombastus von Hohenheim, que adotou o apelido de Paracelso.

–
Paracelso não era apenas um alquimista tentando desvendar os mistérios da matéria, ele era também médico e cirurgião e não tinha medo de desafiar o conservadorismo da época. Não tinha receio de associar a medicina à alquimia para preparar novas poções e remédios, tanto é que criou uma cura que não só salvou a vida de pessoas, como também foi consagrado como dissidente por isso. Esse alquimista propôs uma ideia revolucionária, sugerindo que o mundo era composto por três elementos: sal, enxofre e mercúrio, os vendo como os ingredientes essenciais para produzir tanto metais quanto medicamentos. Ele concluiu que os sais curavam feridas, que o enxofre era combustível e o mercúrio, conhecido à época como azougue (quicksilver, em inglês, quase como aquela marca de roupas), era fluido e volátil.

–
(07:00) Neste momento, o apresentador faz um teste com o mercúrio, tenta levantá-lo, mergulha sua mão utilizando uma camada tripla de luvas, põe um parafuso em cima e por causa da densidade do mercúrio, o parafuso flutua. Fala um pouco desse metal e sua raridade aqui na Terra, mas comenta que pode ser obtido ao aquecer uma rocha vermelha, a cinabarita. Além disso, ele também afirma que nas minas da América do Sul, os garimpeiros arriscavam a sua vida utilizando mercúrio tóxico para extrair outro elemento: o ouro!

–
(09:12) Paracelso não conseguiu convencer as autoridades a respeito de suas ideias sobre os três elementos, mercúrio, enxofre e sal. Na realidade, ele as enfureceu ao ignorar os textos médicos e criar curas alquímicas! Ele era muito radical para sua época. Em um gesto dramático, para mostrar seu desprezo com as autoridades médicas, ele queimou seus livros. Posteriormente, foi forçado a deixar a Universidade da Basileia e fugir para a Alemanha, onde continuou a praticar a medicina e a alquimia.

–
É importante considerar que ele preparou o terreno para uma nova era de questionamentos, numa época em que muitos alquimistas estavam mais interessados em produzir ouro. Aqueciam metais em fornalhas ardentes, ferviam, destilavam… E foi a procura pelo ouro que levou ao primeiro grande avanço na caçada para descobrir os elementos.

–
(10:25) Para os alquimistas, o ouro era como o “cálice sagrado”. Acreditavam que ele possuía propriedades espirituais, mágicas e até mesmo medicinais. Era o símbolo do poder, a cor do sol. Transformado em coroas e moedas, adornava reis, rainhas, palácios e templos há milhares de anos. No Egito antigo, o ouro era a pele dos deuses e para a civilização inca, o ouro era o suor do sol.

–
Os alquimistas ainda não sabiam o que era um elemento, mas alguns foram levados à ideia de que poderiam estar ocultos em outras substâncias quando sugeriram que o ouro poderia estar oculto no corpo humano. A busca constante por conta dessa obsessão levou um alquimista a se tornar a primeira pessoa a descobrir um novo elemento: Henning Brand.

–
Lembram de Vídeos ‘De Onde Vem?’ no Ensino de Química que escrevi, onde eles comentaram sobre ele? 🙂
Ele procurava um meio de extrair ouro de um corpo, quando se deparou com o que parecia ser uma boa ideia: um líquido dourado com estoque abundante – a urina! Em 1669, no escuro e fedorento porão de sua casa em Hamburgo, as caras experiências de alquimia de Brand estavam dilapidando rapidamente as reservas de sua rica esposa, Margaretha. Mas agora, com a urina na mente, Brand acreditava estar à beira de uma fenomenal descoberta. Ele estava prestes a fazer fama e reestabelecer sua fortuna. Tudo que ele precisava era de mais de 50 baldes de urina.

–
(11:26) O apresentador se encontra, então, com o químico Dr. Andrea Sella que estuda o trabalho de Brand e juntos tentam encontrar esse elemento oculto por meio de um experimento. Segundo o pesquisador, Brand tentava chegar ao núcleo da matéria. Começou fazendo ebulição, para se livrar das partes menos importantes, que é claro, era principalmente água.

–
O apresentador pergunta qual era a conexão que possivelmente Brand fez com a urina e o ouro e o pesquisador diz que um dos conceitos da alquimia era de que o homem era um microcosmo do Universo e, portanto, a urina conteria energia vital. A energia da vida. Como um símbolo metafísico da vida, uma substância de poder.
Brand estava tão determinado em encontrar o ouro que destilou a urina até que virasse uma pasta, depois aqueceu por vários dias. No final, vestígios da fumaça revelaram minúsculos fragmentos que queimavam ao ar. Mas o que era esta substância inflamável? Não era dourada como o sol, mas queimava com mais luminosidade que uma vela medieval.
Então, o apresentador e o químico mostraram o que Brand isolou da urina com seus experimentos: fósforo! Ele tinha descoberto este elemento acidentalmente, um elemento jamais visto pela sociedade.

–
Ele procurava por riquezas, mas não percebeu que havia descoberto um conceito fundamental. Que os elementos poderiam estar escondidos em um mundo oculto.
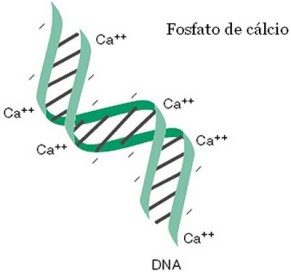
De acordo com o químico, o fósforo é um elemento biologicamente importante. Se lembrarmos que os ossos são compostos especialmente de hidrofosfato de cálcio. Há muito fosfato. Está em nosso DNA, está em cada tecido. Como resultado, há sempre fosfato no sangue e o excesso é transferido para a urina. Um pouco menos de 1 g por L. Este material é altamente instável. Pode-se ver na hora que a fumaça começa a pairar no ar. É um aviso do que irá acontecer se não lidarmos depressa com ele.
–
Então eles o colocam num recipiente, que está cheio de ar e o depositam sobre areia para evitar que o calor afete o vidro. Depois, ele toca o fósforo com uma vareta de vidro aquecida.

–
Por ter brilhado tão intensamente e ser frio o bastante para segurar, Brand batizou sua descoberta de Icy Noctiluca, “a fria luz da noite”.
(16:30) Fósforo. Está em todas as células do corpo humano. É usado em medicamentos para promover o crescimento ósseo, tratar doenças como a osteoporose. 153 milhões de toneladas de fósforo são produzidas todos os anos. Seu fosfato é consumido como suplemento alimentar e é ingrediente para a pasta de dente. Mas ingerir apenas 100 mg de puro fósforo, o suficiente para cobrir a ponta do dedo, pode ser fatal.

–
Ele tem até um lado obscuro. Na Segunda Guerra Mundial, o fósforo foi usado nas milhares de bombas lançadas em Hamburgo, a cidade onde Brand o descobriu!

–
(17:24) Brand esperava que o fósforo o tornasse rico, mas seu dinheiro acabou e ele vendeu o segredo de sua descoberta por um preço vil. Em pouco tempo, o fósforo circulava pelas cortes europeias e em 1677, ele chegou à corte do rei Carlos II. Não demorou, e o rico alquimista Robert Boyle testemunhou sua mágica luminosidade e decidiu investigar suas propriedades.

–
O químico e o apresentador seguiram as instruções do próprio Boyle para tentar uma das suas mais expressivas experiências com o fósforo. Eles dispunham de trechos do livro de Robert Boyle, Novas Experiências e Observações baseadas no ‘Icy Noctiluca’: Misture tudo com meio grão da substância de Noctiluca seca, e seis vezes seu peso em flores de enxofre comuns. Então eles colocaram pó de enxofre. Após, o livro dizia para pôr essa mistura na dobra de um pedaço de papel branco e esmagar com o cabo de uma faca. Observaram que começava a esfumaçar e a acender um pouco de fogo até que o papel entrou em combustão.
Desse modo, eles basicamente recriaram o precursor do palito de fósforo. Isso transformaria radicalmente as coisas, pois se tinha fogo à disposição.

–
Boyle havia se deparado com o ingrediente essencial de um fósforo. Uma grande indústria foi criada a partir desta única experiência. Mas Boyle não estava interessado no potencial econômico do fósforo. Compreender as propriedades deste elemento foi recompensa suficiente para ele. Enfim, o fósforo tinha o poder de transformar. Ele pode não ter transformado chumbo em ouro, mas transformou um alquimista no primeiro químico moderno. Boyle havia preparado o cenário para os futuros caçadores de elementos. Diferentemente dos alquimistas, ele compartilhava seus métodos e foi capaz de passar adiante as ferramentas necessárias para ajudar a desvendar os mistérios da matéria.
(20:25) Al-Khalili foi pesquisar nos cofres da Sociedade Real de Londres algo depositado ali em 1661, apenas um ano após a fundação desta sociedade. O quê? O Químico Cético, escrito por Robert Boyle, que foi um dos fundadores da Sociedade Real.

–
Dra. Anna Marie Roos, especialista na História da Química, estudou a obra de Boyle. Ela diz que esse livro é importante porque é considerado um dos livros que representam a transição da alquimia para a química, e alguns estudiosos o consideram o primeiro livro de química. Ter sido escrito em linguagem simples também foi algo novo.
Segundo o apresentador, basta comparar o livro de Boyle aos escritos enigmáticos de outro alquimista, o grande homem da Ciência, Isaac Newton, para apreciar sua inovação. Segundo a historiadora, o que Boyle fez foi diferente, porque ele estava disposto a divulgar alguns dos seus segredos químicos para o bem da comunidade científica.

–
(22:12) Al-Khalili diz que Boyle estava retirando a alquimia das sombras, para uma era racional e culta. Ele estava expondo o método científico para que todos vissem. Os alquimistas temiam que ele estivesse revelando seus segredos, mas ele não estava interessado em desacreditar a alquimia, mas em livrá-la da sua carga metafísica e substituí-la por uma abordagem mais científica.
(22:44) Uma nova era da experimentação científica havia começado. E com o intercâmbio mais aberto de ideias veio a rejeição da tradição. Ela anunciava uma era na qual as antigas doutrinas gregas eram reavaliadas e novos conceitos introduzidos. Copérnico desafiou a antiga ideia de que a Terra era o centro do Universo, propondo que ela era apenas um dos vários planetas que orbitam o sol. Versálio mapeou o corpo humano. Era uma época empolgante e libertadora, na qual a Europa saíra da Idade das Trevas para a idade da razão.

–
Mas só porque as pessoas estavam pensando diferente, não significava necessariamente que estavam acertando. E embora uma nova geração de cientistas estivesse disposta a descobrir elementos modernos, para substituir os 4 antigos, seu entusiasmo não impediu que adotasse teorias totalmente falsas. E foi assim que a ciência entrou em um dos maiores becos sem saída da História da Química.
(24:05) Era 1667, um ano após o grande incêndio de Londres arrasar uma das maiores cidades da Europa. Os mistérios do fogo estavam no centro das preocupações. Mas ninguém sabia o que era o fogo ou como ele era criado. O químico alemão Johann Becher propôs que o poder destrutivo do fogo era causado por uma entidade chamada flogisto. Acreditava-se que uma substância inodora, incolor, insípida e leve fazia as coisas queimar, reduzindo-as a sua verdadeira forma. Uma madeira em chamas produz cinzas. Assim, a madeira devia ser feita de cinzas, lenha pura e flogisto.

–
O conceito de flogisto parecia tão crível no século 17 que consumiu a comunidade científica. Era aceito como verdade, quase paralisando nossa habilidade de descobrir mais elementos e mapear os contornos da natureza. Um grande químico que trabalhava com gases chegou a alegar que o isolou. No mesmo dia, toda semana, durante 50 anos, um cientista bastante peculiar vinha ao jantar da Sociedade Real para discutir as últimas ideias científicas. Henry Cavendish era descrito como ‘o mais rico dos sábios e o mais sábio dos ricos’. Ele era grande acionista do Banco da Inglaterra e tinha ligações com a realeza, mas é surpreendente que ele tenha vindo a um encontro social.

–
Cavendish era muito tímido e vivia quase isolado. Em casa, ele insistia que seus empregados só se comunicassem com ele por escrito. Colegas do clube disseram que ele, muitas vezes, ficava do lado de fora, tentando arranjar coragem para entrar e que ao falar com ele, era melhor olhar vagamente para o ar do que diretamente para ele. Apesar dos sinais do que conhecemos hoje como autismo, Cavendish deu uma contribuição vital à descoberta dos elementos.
(26:35) O apresentador faz experimentos realizados por Cavendish, que o levaram a produzir o gás hidrogênio. Adicionou um metal, o zinco, a um ácido e observou o surgimento de bolhas na superfície do zinco. Henry Cavendish começou a coletar esse gás, que não tinha odor nem gosto e era completamente invisível. Logo percebeu que não era um gás comum. Ele não sabia que tinha descoberto uma nova substância e o elemento hidrogênio em questão. Pensava ter descoberto um novo tipo de ar, diferente daquele que respiramos, e o chamou de ‘ar inflamável‘. Acreditava que seu ar inflamável tinha que ser o misterioso flogisto, principalmente por ser incolor, inodoro e inflamável. No entanto, certamente estava errado. Não notou que tinha isolado um novo elemento. Investigou as características desse novo gás e calculou que ele era 11 vezes mais leve que o ar que respiramos.

–
(28:20) O apresentador faz um experimento com hidrogênio e detergente líquido, criando bolhas de hidrogênio que sobem por um funil. Por conta da densidade deste gás, por ser mais leve que o ar, as bolhas começam a se separar e subir. Então, ateiam fogo. Assim, comentam que isso reforçou a ideia para Cavendish de que o gás era o flogisto e por isso ele não recebeu os créditos pela descoberta do hidrogênio.
(29:11) Hidrogênio, produzido logo após o Big Bang juntamente com hélio e lítio, é o elemento mais abundante do Universo. A energia solar provém da fusão nuclear do hidrogênio, o mesmo princípio utilizado na bomba de hidrogênio. A natureza altamente inflamável do hidrogênio foi testemunhada quando ele incendiou o Zepelim Hindenburg em 1937 matando 36 pessoas.

–
(30:05) Como muitos caçadores de elementos, Cavendish não notou a importância de sua descoberta, mas ele observou algo que teria papel crucial na nossa compreensão da natureza. Sempre que ateava fogo ao gás descoberto, observava a formação de um líquido na superfície do vidro: água. Isso teve incríveis implicações no século 18, pois na época acreditava-se na antiga ideia grega de que a água era um elemento. Se a água podia ser produzida a partir de dois outros componentes, então ela não poderia ser um elemento. De fato, a água era um composto.
Isso foi um golpe mortal no antigo conceito dos 4 elementos. As observações de Cavendish poderiam ter abalado as bases da crença aceitam, mas não abalaram, pois ele se deixou levar pelo flogisto. Afirmou que os gases deviam conter uma forma de água, modificada pela presença do flogisto. Não ocorreu a ele que a água era um composto.

–
Embora estivesse perto de destruir o templo dos 4 elementos antigos, ele ainda não podia contestá-los. Os pilares desse templo agora estavam em terreno instável, e não demoraria muito para eles ruírem. No entanto, não foi a água de Cavendish que acabaria por refutar a antiga teoria grega, foi o ar.
(31:50) 19 do que chamamos agora de elementos haviam sido descobertos até então, mas os cientistas do século 18 ainda lutavam para decifrar do que o mundo era feito. A Sociedade Real designou seus membros para investigar os gases invisíveis. Na metade do século 18, havia três tipos de ares, ou gases: havia o ar comum, que respiramos; o ar inflamável, conhecido como hidrogênio; e o ar fixo, dióxido de carbono. Fazer experiências com esses ares era o passatempo predileto do clérigo e químico amador Joseph Priestley.

–
Priestley vivia perto de uma cervejaria e passava muito tempo por lá, sobretudo considerando que ele era um pastor unitarista, conhecido por seus sermões. No entanto, ele não estava lá atrás de cerveja, estava interessado no gás produzido no processo de fermentação. Ele o chamou de gás de cervejaria, mais conhecido na época como ar fixo e hoje como dióxido de carbono.
(33:16) O apresentador está numa cervejaria e mostra o dióxido de carbono produzido dentro de um tanque. Este gás, por ter maior densidade que o ar, sai do tanque e se deposita embaixo, mais perto do chão. Nós não conseguimos vê-lo, mas com a experiência realizada por Priestley, foi observado que o dióxido de carbono fazia uma chama acesa apagar. Ele estava tão fascinado pelo ar fixo que o misturou à água, criando a primeira bebida efervescente, a primeira água com gás.

–
(34:15) Sua paixão pela ciência o levou a um convite para a Casa Bowood, em Wiltshire, para ensinar os filhos do futuro primeiro-ministro, Lorde Shelburne. Priestley não tinha a riqueza de químicos como Boyle e Cavendish. Ele ganhou pouco dinheiro com sua invenções e artigos radicais. Lorde Shelburne oferecia a ele estabilidade financeira e a chance de continuar com suas experiências em troca do ensino. Assim, ele se tornou o primeiro químico profissional assalariado. Então, o vídeo mostra onde ele continuou com suas experiências gasosas.
Em 1º de agosto de 1774 Priestley realizou uma das experiências mais importantes da História da Química. Ele estava obstinado a revelar os segredos elementares dos gases. Nessa ocasião, ele começou com um pó conhecido como cal de mercúrio, o óxido de mercúrio. Assim, o apresentador reproduz o experimento. Põe essa substância em um tubo de ensaio para recolher qualquer gás que ela pudesse liberar quando aquecida. Então, ele enche o tubo com mercúrio que aprisionaria o gás liberado. Assim, ele põe o dedo no orifício do tubo e o vira, a fim de que a substância seja submersa no banho de mercúrio. Posteriormente, o pó de óxido de mercúrio fica no topo do tubo. Então, Priestley, bem como o apresentador, aqueceram o pó e perceberam que o nível de mercúrio no tubo estava descendo, pois estava sendo produzido um gás que empurrava o mercúrio para baixo. Isso porque o óxido de mercúrio estava sendo dissociado em seus dois componentes.

–
Em seguida, o apresentador verá qual substância Priestley produziu. Para isso, pegou uma brasa incandescente e mergulhou nesse gás. O resultado? Uma chama intensa foi produzida. Hoje sabemos que o que Joseph Priestley descobriu foi o oxigênio. No entanto, devido à sua crença na ideia do flogisto, achou que a brasa incandescente havia introduzido flogisto no ar novamente e por isso havia pegado fogo. Ele concluiu que seu ar não tinha flogisto e o batizou de ar deflogisticado.
Suas experiências com o novo ar não pararam por aí, ficaram mais estranhas, na verdade. Priestley pôs um rato de um recipiente fechado cheio de seu novo ar esperando que ele sobrevivesse por apenas 15 minutos. No entanto, ele o achou bem vivo depois de meia hora. Assim, ele mesmo inspirou o ar e registrou “Senti meu peito leve e fácil após algum tempo. Dá para se dizer que com o tempo este ar puro pode tornar-se um artigo de luxo. Até agora, só dois ratos e eu tiveram o privilégio de respirá-lo“. Mas sabia ele que todos tinham o privilégio de respirá-lo.

–
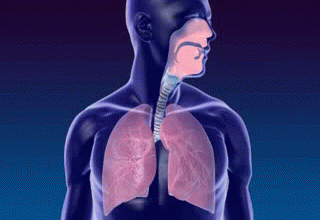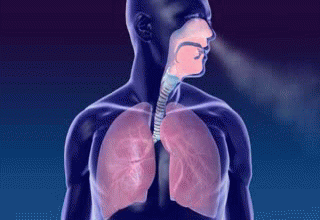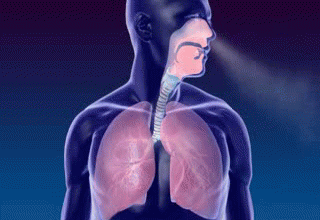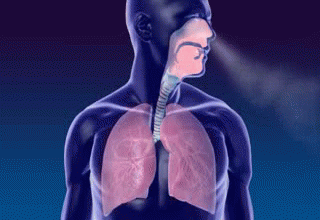
(37:40) Oxigênio é o terceiro elemento mais abundante no Universo, compõe mais da metade do peso de um corpo humano e a -183ºC ele se condensa em um líquido azul pálido. A fundição do aço usa mais da metade do oxigênio produzido comercialmente no mundo. Ele também é usado em combustível de foguetes. Cerca de 21% do ar é oxigênio. Um pouco menos e não poderíamos respirar. Um pouco mais e qualquer matéria orgânica acesa queimaria sem controle.
–
Embora Priestley soubesse que tinha descoberto algo especial, ele não percebeu que havia isolado essa substância composta por um tipo de elemento. Ele ainda estava influenciado por sua crença no flogisto. No entanto, seu caminho estava prestes a cruzar com o de um visionário que também pensava em gases e ares.
(38:54) Em outubro de 1774, Priestley acompanhou seu benfeitor, Lorde Shelburne, numa viagem pela Europa. Eles se dirigiram a Paris, onde foram convidados a jantar com alguns dos mais proeminentes cientistas do país. Deve ter sido um evento e tanto para alguém humilde como Priestley. Um dos convidados foi o famoso cientista Antoine Lavoisier. Aos 28 anos, já tinha sido eleito para a Academia Francesa de Ciências. Esse homem publicou de tudo, desde a mineralogia dos Pirineus até a localização dos melhores abatedouros de Paris.

–
Lavoisier não era apenas membro da emergente elite científica, mas coletor de impostos e membro extremamente rico da burguesia. E também estava determinado a decifrar os mistérios da natureza.
Quando Lavoisier e Priestley encontraram-se num jantar, falaram de Química. A conversa logo girou em torno da nova descoberta de Priestley, o ar deflogisticado. Lavoisier, intrigado, pressionou-o atrás de detalhes e Priestley o achou um ouvinte muito atencioso, pois ele lhe contou tudo sobre sua experiência.

–
Lavoisier e Priestley não tinham nada em comum. Lavoisier tinha o laboratório mais bem equipado da Europa, com mais de 10 mil peças de tecnologia de precisão. Priestley trabalhava num laboratório improvisado, com equipamentos que ele criava. Lavoisier pesava, media, repesava e calculava com precisão antes e depois de cada reação e aplicou essa abordagem para investigar o grande mistério do flogisto.

–
Falando nesse laboratório, futuramente farei um post sobre lugares para visitarmos, caso façamos uma viagem para a região desses lugares que apresentarei. O que acham? 😀
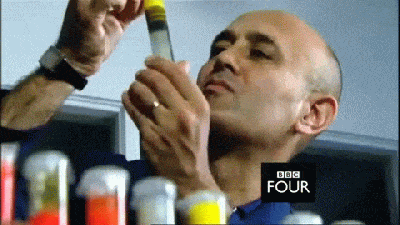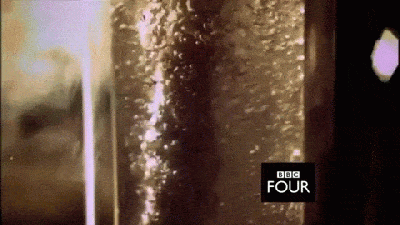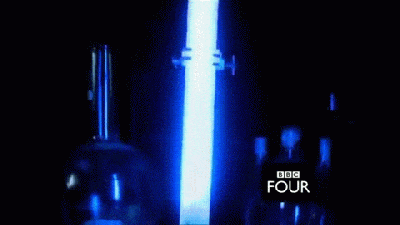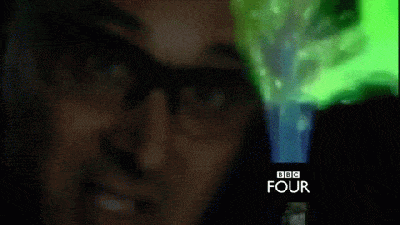
(41:00) A descoberta de Lavoisier surgiu quando ele voltou sua atenção ao detalhe do peso das substâncias, antes e depois de elas serem aquecidas. Al-Khalili reproduz um de seus experimentos. Primeiramente, Lavoisier pesou com precisão um metal. No seu caso, o estanho. No caso do vídeo, pesou-se 150,07 gramas. Em seguida, aqueceu com um maçarico o estanho e depois o repesou. Assim, revelou um problema recorrente com a teoria do flogisto. Se o flogisto é liberado quando uma substância é aquecida, ela deveria pesar menos. No entanto, o que foi observado no vídeo é a massa de 153,64 gramas. Ou seja, quase 4 gramas a mais do que antes de ser aquecida. Foi aí que Lavoisier teve seu momento de inspiração: talvez o flogisto não fosse liberado ao aquecer uma substância, talvez ela absorvesse algum tipo de ar, por isso seu aumento de massa. No entanto, se isso fosse verdade, o que havia sido acrescentado?
–
Influenciado por sua conversa com Priestley, Lavoisier decidiu repetir a experiência de Priestley em sentido reverso. Ele aqueceu um pouco de mercúrio dentro de um recipiente fechado até ele se transformar em óxido de mercúrio, a mesma substância que Priestley usou em sua experiência. Ele mediu a quantia de ar absorvida pelo mercúrio quando aquecido. Depois, ele aqueceu o óxido de mercúrio e observou que a quantidade de ar liberada foi exatamente a mesma absorvida pelo mercúrio quando aquecido.

–
Num momento de inspiração, ele notou que algo no ar foi absorvido pelo mercúrio para produzir o óxido e o mesmo gás foi liberado em seguida. Ele concluiu que este gás não tinha nada a ver com o flogisto. De fato, era algo totalmente novo. Então, Lavoisier o batizou de oxigênio. Graças à experiência de Priestley, segundo o apresentador, Lavoisier expusera à verdade a mentira que havia destruído a Química durante um século. Enfim, Lavoisier mostrara que o flogisto não existia, libertou a Química dos grilhões do flogisto, os resquícios da visão medieval. Ele foi o pioneiro de um método científico que poderia mapear rapidamente os elementos.
No entanto, para ira de Priestley, Lavoisier alegou que ele descobrira o oxigênio, pois foi quem o reconhecera como um novo elemento. A tentativa de resolver quem deveria receber a glória mostrou ser algo complicado… Uma guerra amargurada de palavras e reputação irrompeu entre a Inglaterra e a França. Priestley alegou que Lavoisier tentou roubar sua ideia, e tinha razão, pois as experiências de Lavoisier com o oxigênio só foram concluídas após o encontro que tiveram. Ele pode não ter descoberto o oxigênio, mas descobriu sua importância. E, de acordo com o vídeo, é Lavoisier, não Priestley, que é conhecido como o pai da Química.

–
(44:38) A descoberta do oxigênio destruiu qualquer vestígio do conceito grego dos 4 elementos. A água era composta de hidrogênio e oxigênio. A Terra e o ar eram uma miscelânea de diferentes elementos. E o fogo, bem, não era um elemento.
A Química entrava na era moderna, uma época em que os químicos decifravam a matéria, faziam grandes descobertas para tentar entender do que nosso mundo é feito. No entanto, parecia não haver nenhuma ordem, nenhuma lógica em suas descobertas: apenas elementos aleatórios espalhados pela paisagem química. Não havia nenhuma Tabela Periódica.

–
Lavoisier foi o primeiro cientista a definir o que era um elemento, uma substância que não poderia ser decomposta através de uma reação química. Eles então mostram o manuscrito original onde ele começou a elaborar a lista definitiva de todos os elementos: 33 substituíam os 4 antigos. Dividiu em 4 categorias, os metais, os não-metais, os gases e os elementos terrosos.
Como ele não acertou tudo, é interessante observar que ele classificou lumiere, luz, e calourique, o calor, como gases e não como formas de energia pura. Apesar desses equívocos, isso a lista elaborada foi um grande avanço para a Química, pois foi a primeira percepção de que houvesse alguma ordem dos elementos, algum imenso padrão para elementos estruturais do nosso mundo.

–
Lavoisier não parou por aí, ele continuou. Criou um sistema para classificar as descobertas de outros químicos e começou a transformar a linguagem da Química. Iniciou a revolução do vocabulário científico, substituindo o pitoresco e o poético por precisão. Assim, o ar deflogisticado tornou-se oxigênio, açafrão de marte adstringente virou óxido de ferro, óleo de vitríolo passou a se chamar ácido sulfúrico e lã filosófica virou óxido de zinco.
(48:00) Em 1789 a Revolução Francesa teria terríveis consequências para Lavoisier e Priestley. Na Inglaterra, a simpatia de Priestley pelo levante trouxe-lhe atenção indesejável. As coisas se agitaram em 1791 quando uma multidão enfurecida, com medo de que a revolução chegasse à Inglaterra foi até a sua casa e a incendiou. Graças a um alerta, Priestley escapou ileso, mas decidiu fugir para os Estados Unidos. Lavoisier não teve tanta sorte. Apesar de seu trabalho para o governo, ele e outros 28 coletores de impostos foram julgados e condenados por conspirar contra o povo francês. No vídeo é possível observar até onde ele foi levado, a Praça da Revolução, onde no mesmo dia, em 8 de maio de 1794 ele foi guilhotinado. Um dia depois, o matemático francês Joseph Legrange comentou: “Bastou um instante para cortar a sua cabeça, mas cem anos não serão suficientes para produzir outra semelhante“.

–
Lavoisier deixou um legado incrível, acabando com o antigo dogma e o substituiu pela abordagem empírica. Não havia mais como voltar atrás. A experimentação agora poderia provar ou refutar a mais radical das ideias. Contudo, os cientistas ainda estavam convencidos da existência de mais elementos e estavam desesperados para descobrir novos meios de revelá-los. A matéria permanecia fundamentalmente impenetrável e seria necessária uma força poderosa e perigosa para descobrir um novo meio para dissociá-la.
(50:04) Eis que surge Humphry Davy, um cientista carismático da Cornualha que frequentemente cortejava o perigo. Ele era professor de Química no Instituto Real de Londres. Em 6 de outubro de 1807 ele trabalhava no porão onde adaptou os aposentos dos empregados num laboratório. Davy trabalhava com alguns sais cristalinos chamados potassa. Lavoisier fora incapaz de dissociá-la e reconhecer o elemento, mas Davy não estava convencido. Ele suspeitava que a potassa fosse composta de mais de um elemento, mas não importava o quanto tentassem, a potassa os derrotava. Não parecia haver forma de a Química dissociá-la. Porém, Humphry Davy teve uma nova ideia: a primeira bateria elétrica acabara de ser inventada. Ela era bem simples. Fileiras de placas de metal e papelão embebidas em água salgada. Mesmo assim, proporcionava a primeira corrente contínua do mundo.

–
(51:20) Então, o apresentador usa o mesmo princípio da época para gerar eletricidade e faz um experimento. Ele tem uma moeda de cobre ligada a um disco de zinco via um fio de cobre. Ao ter o suficiente deles ligando todas as taças cheias de água salgada, ele cria um circuito. Ao conectar a moeda de cobre verifica a geração de eletricidade, acendendo uma luz. Mostra a formação dessa eletricidade usando apenas dois metais distintos, taças com água salgada e uma lâmpada.

–
Conforme afirma o vídeo, a maioria dos químicos da época pensava que o efeito tinha a ver com os metais. No entanto, Davy acreditava que havia algo mais profundo. Que era uma reação química que produzia a corrente elétrica. No entanto, se fosse assim, talvez o inverso fosse verdade e uma corrente elétrica pudesse criar uma reação química. Então, esse químico resolveu descobrir.
(52:00) Neste momento, o apresentador e o químico Hal Sosabowski realizam a experiência de Davy para verificar o que ele realmente presenciou na época. Os homens adicionam a potassa num recipiente de porcelana e a derretem com a chama de um maçarico, já que ela tem um ponto de fusão relativamente baixo: cerca de 360ºC. Quase de imediato, veem um líquido se formando. Discutem que Davy não sabia o que estava procurando, ele não sabia que procurava um metal muito reativo que poderia pegar fogo no ar. Em seguida, pegam a bateria com eletrodos de carbono e cabos de conexão e dissociam a potassa. A corrente elétrica que passa pela potassa derretida cria uma reação química imprevisível e volátil, dissociando as partículas elétricas na potassa. Ocorre, também, o consumo dos eletrodos porque o meio é altamente cáustico. Ao observarem o clarão rosa formado, percebem que o potássio foi produzido, pois ele reage de imediato com o oxigênio na superfície. Assim, Humphry Davy dissociou a potassa em seus ingredientes fundamentais, forçando o surgimento de um elemento jamais visto, o potássio.

–
(55:20) O potássio é um metal leve, prateado e que pode ser cortado como queijo. Por um instante, ele cintila como aço e depois desmancha no ar. Este elemento é essencial para a vida humana, nosso corpo precisa de suprimento constante para manter os músculos e rins funcionando. Ele também ajuda a transmitir os impulsos nervosos. Contudo, ele também mata. Uma grande dose de cloreto de potássio pode resultar em um ataque cardíaco fatal. Quando o potássio toca a água, ele reage explosivamente liberando hidrogênio e deixando para trás potassa. Além disso, ele é abundante como o sal na água do mar.

–
A descoberta do potássio pelo Davy foi apenas o início. Posteriormente, ele acrescentou 6 novos elementos à lista de Lavoisier, e confirmou que cloro e iodo também eram elementos. Segundo o apresentador, ele era um desbravador no mundo da Química, destemido e até mesmo imprudente diante de uma experiência perigosa. Para ele, o perigo fazia parte da área e, provavelmente, foi a inalação dessas substâncias durante sua vida que o matou aos 50 anos em maio de 1829. A sua busca pelo conhecimento, em aprofundar a reflexão sobre o mundo natural oculto talvez tenha custado sua vida. No entanto, o passo que ele deu pela ciência é imensurável. Na época de sua morte, a ideia de elementos estava firmemente estabelecida: 55 dos elementos estruturais do nosso planeta tinham sido identificados e o mundo tinha uma nova ciência: a Química! ❤

–
Bom, então é isso meu povo!
Até semana que vem!
Comenteeem ❤


PARABÉNS PELO SEU TRABALHO. AMEI.
SEMPRE TENTO PASSAR PARA O OS MEUS ALUNOS A HISTÓRIA E COMO O CIENTISTA CHEGOU AO RESULTADO PARA QUE NÃO OCORRA “DECOREBAS”. FICOU COMPLETO AGORA.
FOI FANTÁSTICO VOCÊ COMPARTILHAR CONOSCO.
ABRACOS
Que bom que você gostou, Adriana!!! 🙂 Espero que seja útil 😀 Depois me conta como foram as aulas com o vídeo 😉
OLÀ KAROL!
APÓS O VIDEO O RESULTADO FOI ESPETACULAR.
Que bom!! Fico muito feliz que tenha sido proveitoso!!
Adorei, pretendo usar em sala, esperando ansiosa os cometários do episódio 3.
Valeu a ajuda.
Logo sai! Agora que estou de férias pretendo trabalhar na transcrição dos áudios do episódio 3 hehe
Karol, estou encantada com seu site. E com vc!! Ouvi sua entrevista. Vc dá aulas presenciais certo?Teve ou tem alguma experiência em aulas EaD?
Fico muito feliz, Maria! 😀 Obrigada por ter ouvido a entrevista! 🙂 Não, ainda não dou aulas (só faço estágio mesmo) e participava do Pibid, sabe?
Ainda não li seu resumo, mas se seguir na mesma pegada do vídeo vai ser fenomenal. Não sei se pulei alguma parte que não devia, mas você em algum momento, disponibilizou ou vai disponibilizar o restante dos episódios? Achei interessante demais e gostaria de ver todos ele. Parabéns pelo trabalho, ficou incrível. 🙂
Oi Carlos, obrigada pelo comentário! 😀 Então, você não pulou nada mesmo haha, esse post é uma introdução ao documentário e também um apanhando das informações do primeiro episódio mesmo. Farei sim para os próximos dois episódios! 😀 Só estou terminando outros posts para as próximas sextas primeiramente e depois farei esse levantamento de informações para “A ordem dos elementos” e “O poder dos elementos”. Se quiser seguir a página no face ou seguir por email (se encontram na lateral do site se você lê pelo PC ou no fim da página se você lê pelo celular), fica bem fácil para você ser avisado quando eu postar. 😀 Mas não postarei isso nas próximas semanas já porque demora um pouco para transcrever, e agora que iniciou o semestre, talvez leve umas 3 semanas para fazer isso usando o tempo livre que tenho… Mas não desista desse post, em breve sai! haha
Como conseguir este testo importante
Na seção ‘downloads’ no início do post, ou pode clicar aqui: https://quimicaempratica.files.wordpress.com/2016/02/versc3a3o-downlod-ep-1.pdf . Essa é a versão pra download sem imagens 😉
Muito interessante a relacionar a química e a história. parabéns pelo trabalho!
Karoline, adorei o post, o documentário e o liiindo resumo que vc fez. Também fiquei com muitas informações soltas na minha cabeça e o resumo foi crucial para guardar os pontos mais importantes do documentário. Meus parabéns pelo blog e muito obrigada por compartilhar seu conhecimento conosco.
Que bom que gostooou, Cheisy! Pois é, é muita coisa interessante no documentário, né? Futuramente farei esse resumo para os episódios 2 e 3 dessa série, que são igualmente maravilhosos. ❤
Parabéns pelo trabalho e mto obrigada por disponibilizar!
Perfeito para as primeiras aulas em um colégio novo, onde quero iniciar o ensino da química com uma abordagem diferente da tradicional!
Ainda não conhecia o blog, vou aproveitar para explorar! 😍😘
Que bom que gostou! Sim, acho que pode ser útil mesmo nas aulas esse vídeo. Seja bem-vida, então, hehe. O blog é novo ainda, mas aos poucos ele vai tendo mais conteúdo ♥. Qualquer sugestão é bem-vinda também! Depois volta aqui e me conta como foi a aula. Todos adorariam ler os comentários também 🙂
Parabéns, ficou maravilhoso. Adoro o blog.
Que bom que gostou! Obrigada pelo comentário e por gostar do blog!!! 😀
Bacana. parabéns. Sou apaixonado por documentários e fico muito feliz em ter este trabalho disponibilizado.
Que bom que gostou! 😀 Obrigada pelo comentário. Se tiver alguma sugestão de outro documentário legal, me avisa. 😉
A gente aprende através desse vídeo a Química é uma história volátil, precisamos entender também ela é uma ciência que estuda as transformações que envolvem matéria e energia
É verdade, né?
Esse ano ainda sai o último episódio e a transcrição de outros documentários 😊